文章來源:蓋德化工網
賽道有放量需求、競品做得好,不代表可以盲目放大后入局新藥和仿制的市場預期。

原研市場還沒焐熱,原料藥全國首家轉A的首仿就要來了
Guide View
近期,CDE官網顯示,四川科倫的“蘆曲泊帕”API激活轉A,為全國首家。齊魯緊隨其后,預計過幾個月會有相關更新;原研則未在平臺做相關登記。
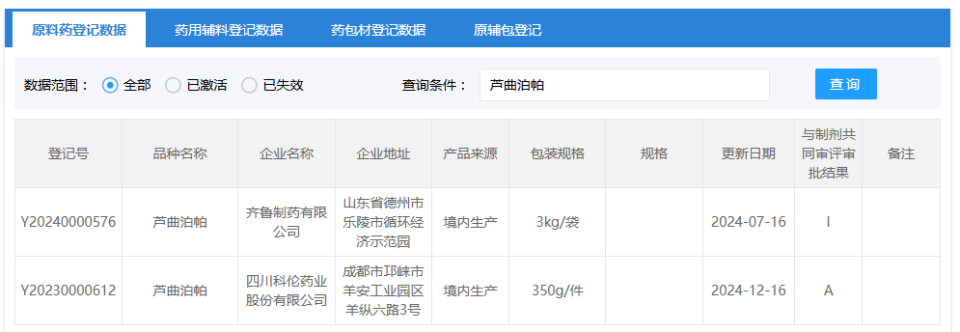
“蘆曲泊帕”原研企業是鹽野義(Shionogi)制藥,2019年,億騰醫藥與鹽野義制藥達成協議,獲得了該藥在中國大陸、港澳地區的產品開發和商業化權利。去年6月,進口原研產品按5.1類在華獲批,商品名蘆曲泊帕(穩可達?),適用于成年患者,患有慢性肝病伴血小板減少癥,且計劃接受手術(包括診斷性操作)。
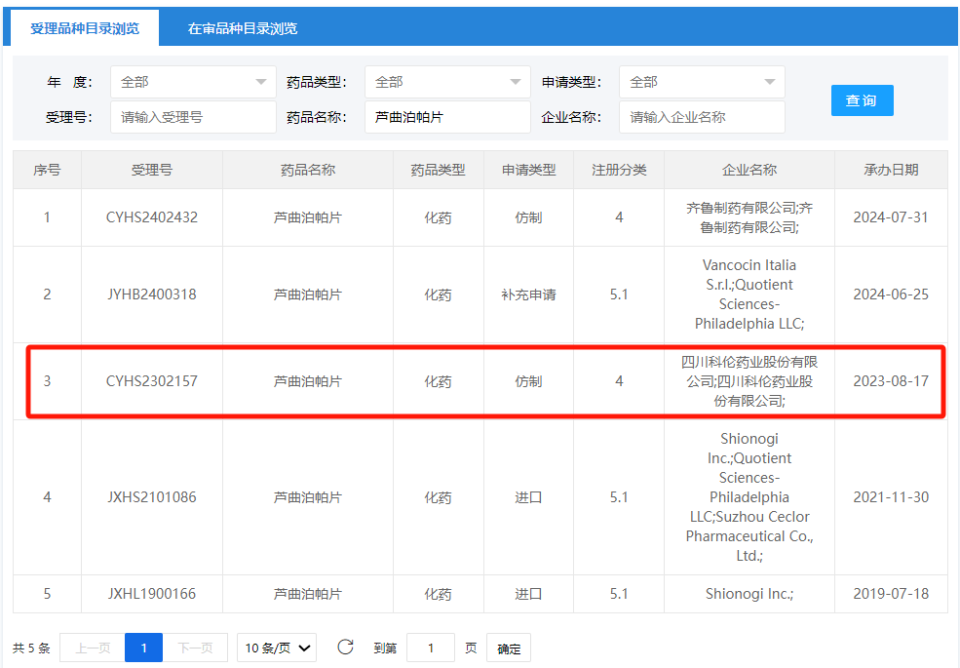
原研獲批后僅兩個月,CDE官網就顯示同年8月已受理科倫藥業的仿制上市申請。如今API先行轉A,業內人士推測科倫藥業“蘆曲泊帕”制劑首仿或將獲批。
這意味著蘆曲泊帕片很快就會進入仿制競爭時代。該藥品的核心化合物專利已于今年年中到期。
值得關注的是,隨著仿制行業競爭加劇,藥企扎堆搶仿立項,加速集采化進程,首仿公司賺錢的窗口期快速縮短,搶仿也被迫不斷提速升級,2023年以來已出現多款原研前腳在華上市,后腳仿制立刻申報的情況,除了蘆曲泊帕,類似的還有:布地奈德腸溶膠囊(耐賦康?/Nefecon?)、布瑞哌唑片(商品名:銳思定)。
賽道仍有放量空間,但后入局新品仿制有巨大不確定風險
Guide View
如上文所述,“蘆曲泊帕”在華獲批的適應癥是用于計劃接受手術(含診斷性操作)的慢性肝病伴血小板減少癥的成人患者。世衛組織數據顯示,中國各類肝病患者總數超過4億,其中乙肝患者接近1億,慢性肝病成人患者約1360萬。在慢性肝病患者中,血小板減少是一個普遍問題,發生率高達70-80%。這種情況主要是由于肝功能改變導致血小板生成素(TPO)的產生減少或活性降低所致。
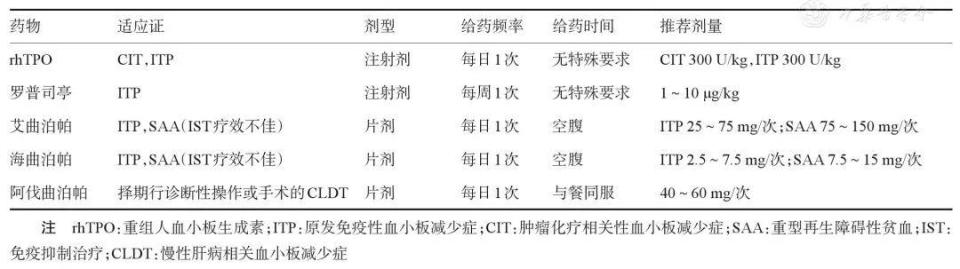
對癥治療上,可采用促血小板生成藥物,包括重組人血小板生成素(rhTPO)和血小板生成素受體激動劑(TPO-RA),其通過特異性結合血小板生成素(TPO)受體,調節巨核細胞增殖、分化與成熟,促進血小板生成。
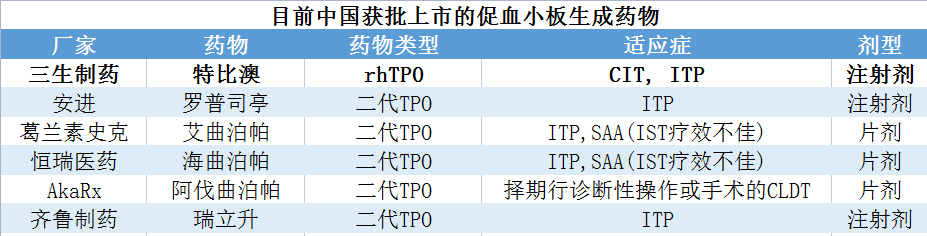
目前全球已有6種促血小板生成藥物獲批進入臨床應用,包括rhTPO、羅普司亭(Romiplostim)、艾曲泊帕(Eltrombopag)、海曲泊帕(Hetrombopag)、阿伐曲泊帕(Avatrombopag)及蘆曲泊帕(Lusutrombopag)。
包括蘆曲泊帕在內,一款藥物可以通過不斷擴展多個適應癥、擴寬用藥群體,不斷實現銷售放量,比如:
全球唯一一款商業化的重組人血小板生成素(rhTPO)產品“特比澳”,最早于2005年獲批上市,在2007年納入國家醫保,已獲批成人實體瘤化療后血小板減少癥(CIT)和成人原發免疫性血小板減少癥(ITP)適應癥,2023年銷售額達到42.05億元,同比增長23.8%,成為國內大分子藥物銷售額第一的品種。
其他幾款先于蘆曲泊帕在國內上市的產品,銷量亦是不錯,比如艾曲泊帕2022年中國銷售額超7億、海曲泊帕2023上半年中國銷售額超4億元,同比增長約167%、阿伐曲泊帕2022年中國銷量超6億元,同比增長166.42%。
目前,蘆曲泊帕上市才一年多,尚未拓展多適應癥,其全球銷量與國內市場銷量更是未見很好的數據披露,不過作為新一代TPO激動劑,蘆曲泊帕依然具有顯著優勢:安全性更高、口服給藥更便捷、無免疫原性問題,且不受食物影響,藥物相互作用少。這些特點不僅確保了治療效果的穩定性,也為患者提供了更靈活的用藥方案。
這款藥物除了億騰醫藥引入原研,國內科倫沖刺首仿,齊魯緊隨其后,至少是看中血小板減少癥治療領域的“龐大市場”,除了三生制藥,國內藥企渴求進入該賽道的一塊“敲門磚”,無論是通過創新藥還是仿制藥入局,只要藥企操盤實力夠,市場空間是有的,比如恒瑞海曲泊帕2023年在中國三大終端六大市場的銷售額超過12億元,同比增長約104%,目前適應癥還在增加中……
賽道雖然還有持續做大的機會,但入局蘆曲泊帕仿制的藥企將要面臨共同挑戰:
那就是這款新藥,作為后入局者,能否成功在國內不斷擴展適應癥,不斷做大市場,其中包括針對慢性肝病成人患者血小板減少癥治療市場的成功培育。同時海外市場上市多年,仍沒有該款新藥較好的銷售數據可供參考,不確定的市場放量,需要藥企承擔巨大風險,極其考驗操盤能力。
