文章來源:藥智新聞
全球新藥2025年1月進(jìn)展概述
1.1 進(jìn)展到最新階段的重點(diǎn)項(xiàng)目
1月共676個(gè)藥物有相關(guān)更新動(dòng)態(tài),其中有309個(gè)項(xiàng)目推進(jìn)到最新的階段,其中在中國境內(nèi)進(jìn)行的項(xiàng)目共216個(gè),境外項(xiàng)目有93個(gè)。
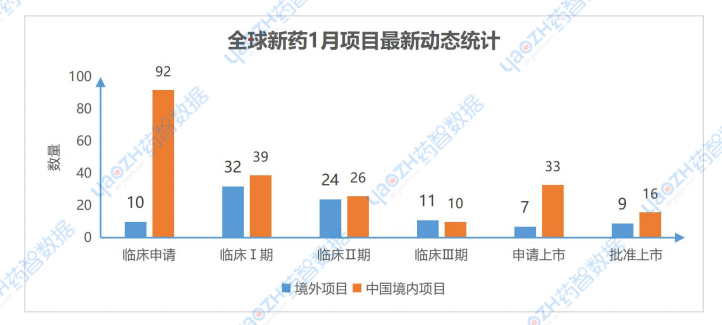
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
1.2 研發(fā)前十靶點(diǎn)
1月有更新動(dòng)態(tài)的676個(gè)項(xiàng)目中,涉及最多的靶點(diǎn)是GLP-1R,其次是PD-1和PD-L1,以下是排名前十的靶點(diǎn),圖中僅展示藥品總數(shù),具體藥品內(nèi)容可通過全球藥物分析系統(tǒng)進(jìn)行查看。
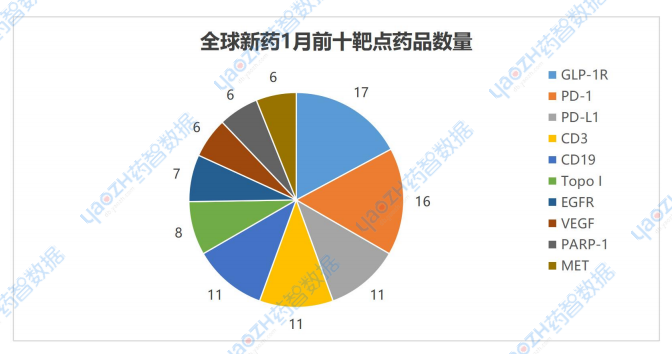
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
1.3 研發(fā)前十適應(yīng)癥
1月有更新動(dòng)態(tài)的676個(gè)項(xiàng)目中,涉及最多的適應(yīng)癥是實(shí)體瘤,其次是晚期實(shí)體瘤和非小細(xì)胞肺癌,以下是排名前十的適應(yīng)癥及其全球最高研發(fā)階段情況,圖中僅展示藥品總數(shù),具體藥品內(nèi)容可通過全球藥物分析系統(tǒng)進(jìn)行查看。
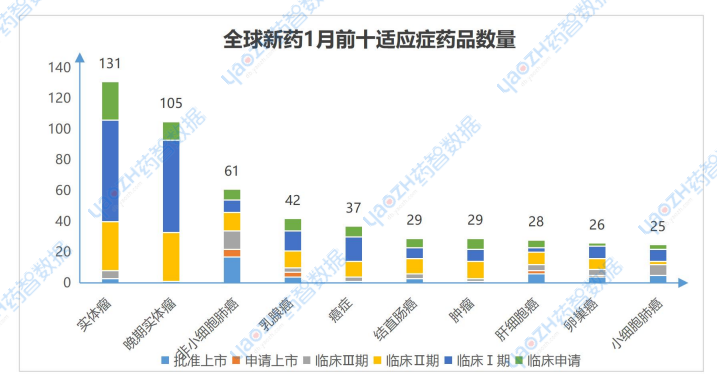
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
1.4 研發(fā)前十藥品類別
從成分類別分析,1月有最新進(jìn)展的相關(guān)藥品占比前三的分別是化藥59%,抗體17%,細(xì)胞5%。
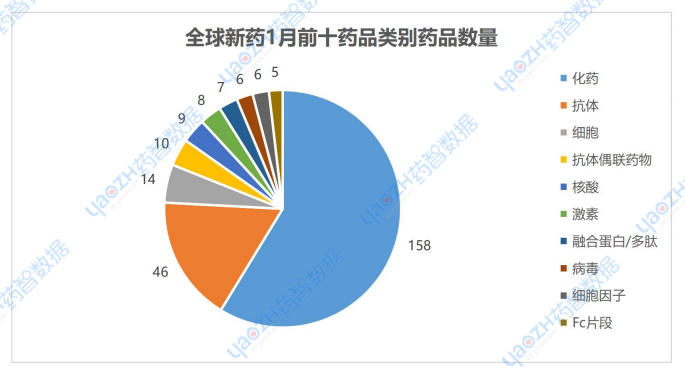
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
全球新藥2025年1月重點(diǎn)項(xiàng)目
2.1 全球獲批的新藥
據(jù)全球藥物分析系統(tǒng)數(shù)據(jù)庫統(tǒng)計(jì),1月全球共25款藥物獲批上市(包括新獲批適應(yīng)癥),其中境外9個(gè)上市藥品,中國境內(nèi)16個(gè)藥品,下表展示部分重點(diǎn)上市藥物。
更多內(nèi)容前往藥智數(shù)據(jù)公眾號(hào)后臺(tái)回復(fù)【全球新藥】,獲取完整《2025年各月全球新藥研發(fā)進(jìn)展》PDF版及申請/獲批上市藥物清單excel版。
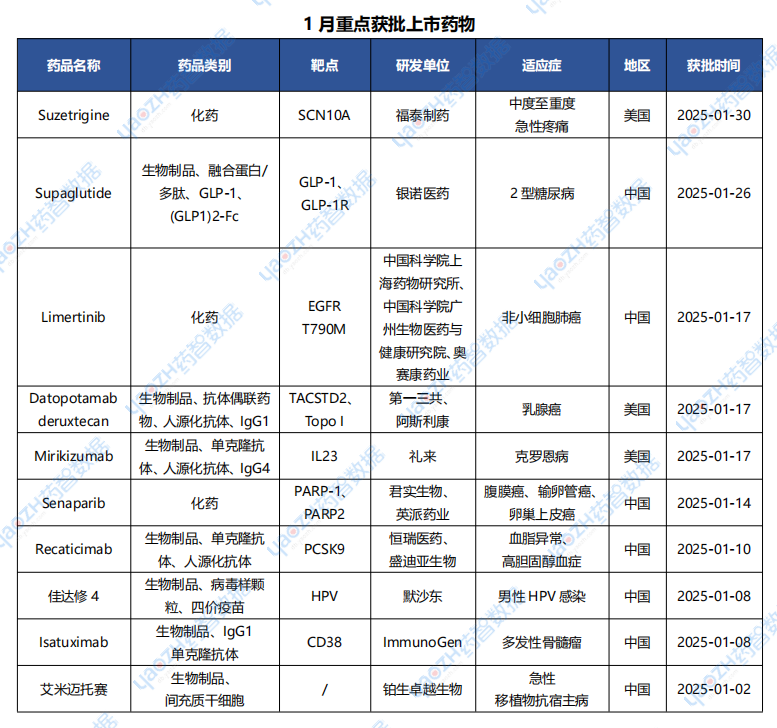
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
2.1.1 Suzetrigine——全球首個(gè)非阿片類止痛藥FDA批準(zhǔn)上市
2025年1月30日,F(xiàn)DA宣布已批準(zhǔn)Vertex公司的創(chuàng)新療法Suzetrigine(Journavx,VX-548)上市,用于治療成人中度至重度急性疼痛。Suzetrigine是一種新型非阿片類鎮(zhèn)痛藥,是全球首款獲批上市的治療疼痛的NaV1.8抑制劑,是美國FDA所批準(zhǔn)的首款基于新機(jī)制的非阿片類止痛藥物,該藥物的獲批將使之成為20多年來首個(gè)用于治療急性疼痛的新機(jī)制藥物。
FDA長期以來一直支持非阿片類止痛藥的研發(fā),并發(fā)布了旨在鼓勵(lì)研發(fā)非阿片類止痛藥治療急性疼痛的指導(dǎo)草案和臨床實(shí)踐指南。據(jù)全球藥物分析系統(tǒng)數(shù)據(jù)庫統(tǒng)計(jì),目前全球共有26款靶向NaV1.8新藥正在研發(fā)當(dāng)中,分別用于各種疼痛包括急性疼痛、慢性疼痛、術(shù)后疼痛、關(guān)節(jié)疼痛等。國內(nèi)市場包括恒瑞、濟(jì)煜醫(yī)藥、海博為藥業(yè)、健康元藥業(yè)也有相關(guān)靶向NaV1.8藥品進(jìn)入臨床早期階段。
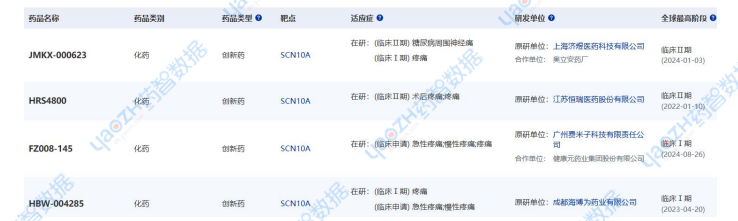
▲國內(nèi)靶向NaV1.8疼痛市場研發(fā)格局
圖片來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
2.1.2 Recaticimab——全球首個(gè)超長效PCSK9單抗國內(nèi)獲批上市
2025年1月10日,中國國家藥監(jiān)局批準(zhǔn)恒瑞醫(yī)藥的注射用瑞卡西單抗(Recaticimab)上市,瑞卡西單抗是恒瑞在心血管疾病領(lǐng)域上市的首個(gè)1類創(chuàng)新藥,其注射間隔可長達(dá)8周,突破了目前國內(nèi)外已獲批的PCSK9單抗需要每2周、4周或6周的注射頻次,是全球首個(gè)超長效PCSK9單抗。
此次獲批上市的適應(yīng)癥為:在控制飲食的基礎(chǔ)上,與他汀類藥物,或者與他汀類藥物及其他降脂療法聯(lián)合用藥,用于接受中等或以上劑量他汀類藥物治療仍無法達(dá)到低密度脂蛋白膽固醇(LDL-C)目標(biāo)的原發(fā)性高膽固醇血癥(包括雜合子型家族性和非家族性高膽固醇血癥)和混合型血脂異常的成人患者;或單藥用于非家族性高膽固醇血癥和混合型血脂異常的成人患者,以降低低密度脂蛋白膽固醇(LDL-C)、總膽固醇(TC)、載脂蛋白B(ApoB)水平。
2.1.3 艾米邁托賽——國內(nèi)首款干細(xì)胞療法批準(zhǔn)上市
2025年01月02日,中國國家藥監(jiān)局批準(zhǔn)鉑生卓越生物的干細(xì)胞療法艾米邁托賽獲批上市,用于治療14 歲以上消化道受累為主的激素治療失敗的急性移植物抗宿主病。這是國內(nèi)首款獲批上市的干細(xì)胞療法,填補(bǔ)了國內(nèi)干細(xì)胞治療的空白。在這款干細(xì)胞產(chǎn)品獲批前不久,2024年12月18日,美國FDA也批準(zhǔn)了第一個(gè)基于間充質(zhì)干細(xì)胞的治療療法Ryoncil(remestemcel-l)用于治療類固醇難治性急性移植物抗宿主病。短短半個(gè)月時(shí)間,中美兩國兩款干細(xì)胞產(chǎn)品相繼獲批,這不僅是干細(xì)胞行業(yè)劃時(shí)代的突破,也是干細(xì)胞治療從技術(shù)時(shí)代邁向產(chǎn)品時(shí)代的關(guān)鍵里程碑。
在所有干細(xì)胞療法中,間充質(zhì)干細(xì)胞療法是最為熱門的類別。據(jù)全球藥物分析系統(tǒng)數(shù)據(jù)庫統(tǒng)計(jì),目前全球共有235個(gè)間充質(zhì)干細(xì)胞項(xiàng)目在研發(fā)階段,處于斷層式領(lǐng)先,而緊隨其后的是造血干細(xì)胞僅有74個(gè)項(xiàng)目,其他還包括脂肪干細(xì)胞、神經(jīng)干細(xì)胞、胚胎干細(xì)胞等多種干細(xì)胞療法均在開展臨床探索研究。
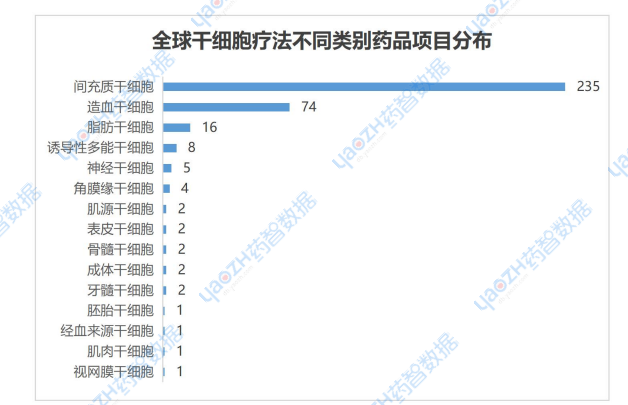
▲全球干細(xì)胞療法不同類別藥品項(xiàng)目分布
圖片來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
2.2 全球申請上市的新藥
據(jù)全球藥物分析系統(tǒng)數(shù)據(jù)庫統(tǒng)計(jì),1月全球共40款藥物申請上市(包括首次申請和新申請),下表展示部分重點(diǎn)申請上市藥物。
更多內(nèi)容前往藥智數(shù)據(jù)公眾號(hào)后臺(tái)回復(fù)【全球新藥】,獲取完整《2025年各月全球新藥研發(fā)進(jìn)展》PDF版及申請/獲批上市藥物清單excel版。
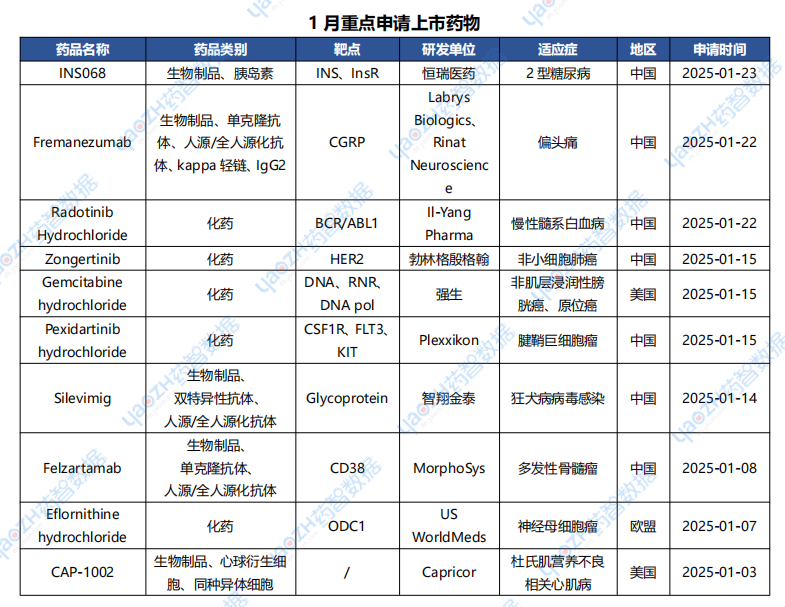
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
2.2.1 Silevimig——全球首款狂犬病雙抗藥物國內(nèi)申請上市
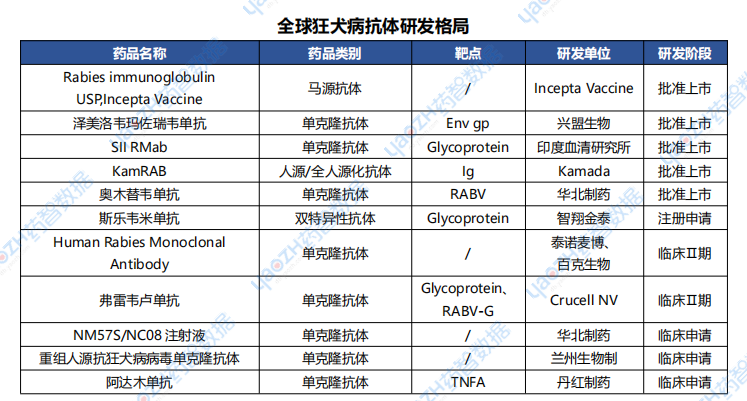
2025年1月14日,據(jù)CDE 官網(wǎng)顯示,智翔金泰1類新藥斯樂韋米單抗(Silevimig,GR1801)在國內(nèi)報(bào)上市,用于疑似狂犬病病毒III級(jí)暴露后的被動(dòng)免疫。如果成功獲批,該藥將成為狂犬病領(lǐng)域全球首款且目前唯一的雙抗藥物。
據(jù)全球藥物分析系統(tǒng)統(tǒng)計(jì),在狂犬病抗體研發(fā)領(lǐng)域共11款藥物進(jìn)入臨床開發(fā)及以上階段,其中有8款單抗、1款雙抗、2款其他抗體。目前國內(nèi)已知獲批上市的僅2款抗狂犬病毒單抗,分別為華北制藥的奧木替韋單抗和興盟生物開發(fā)的重組人源化單抗?jié)擅缆屙f瑪佐瑞韋單抗。
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
2.3 全球新藥重點(diǎn)臨床試驗(yàn)及IND申請
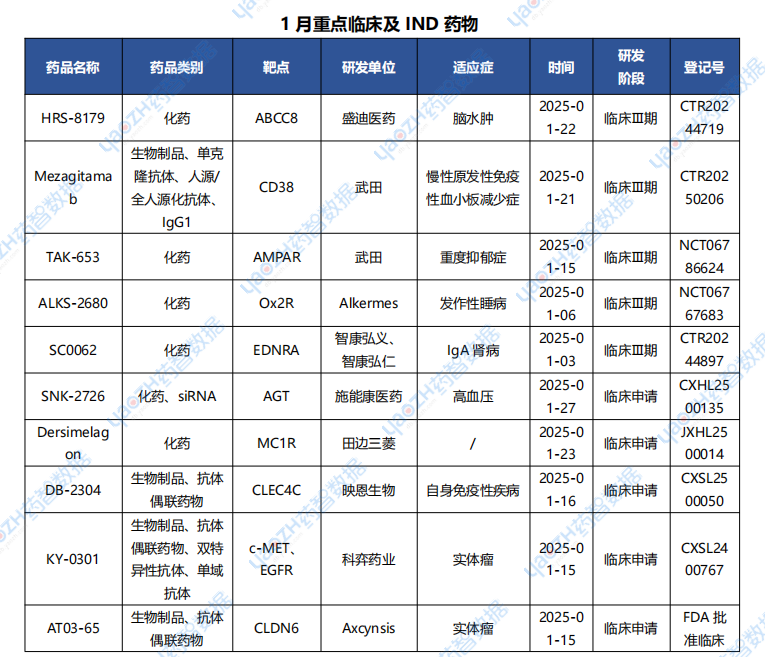
據(jù)全球藥物分析系統(tǒng)數(shù)據(jù)庫統(tǒng)計(jì),2025年1月“首次”進(jìn)入重點(diǎn)臨床試驗(yàn)(三期)的新藥項(xiàng)目有21個(gè),臨床申請有102個(gè),下表展示部分重點(diǎn)信息。
更多內(nèi)容前往藥智數(shù)據(jù)公眾號(hào)后臺(tái)回復(fù)【全球新藥】,獲取完整《2025年各月全球新藥研發(fā)進(jìn)展》PDF版及申請/獲批上市藥物清單excel版。
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-全球藥物分析系統(tǒng)
1月醫(yī)藥交易、投融資及并購事件
據(jù)投資格局?jǐn)?shù)據(jù)庫統(tǒng)計(jì),2025年1月共247條醫(yī)藥交易事件、167條醫(yī)藥投融資事件和43項(xiàng)企業(yè)并購事件發(fā)生,重點(diǎn)交易信息如下,完整清單詳見藥智數(shù)據(jù)企業(yè)版-投資格局?jǐn)?shù)據(jù)庫。
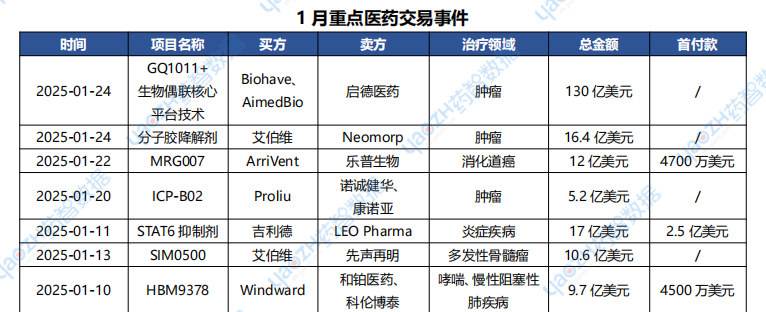
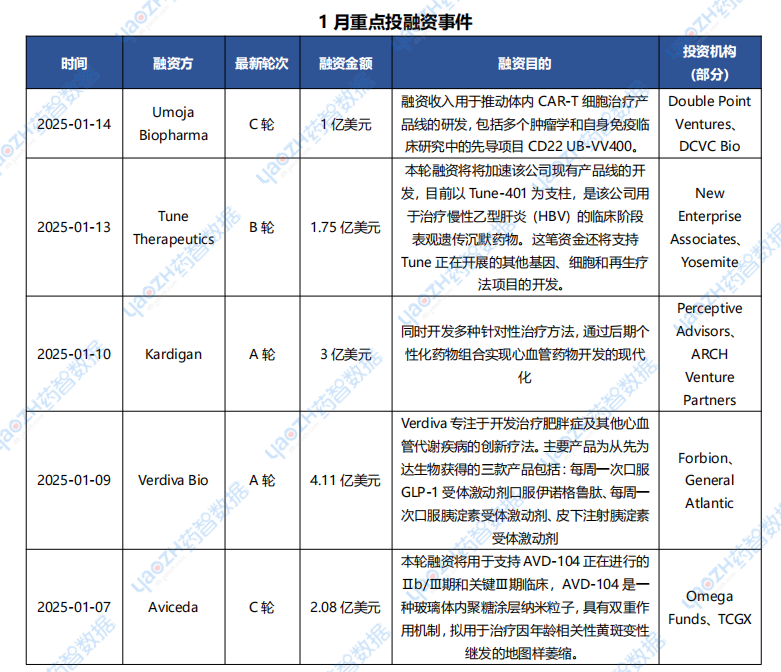
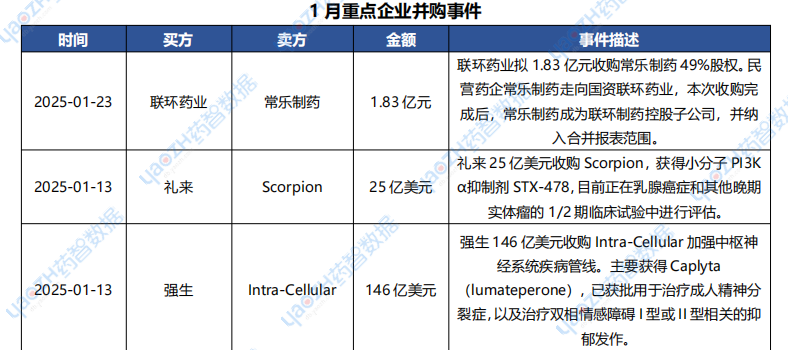
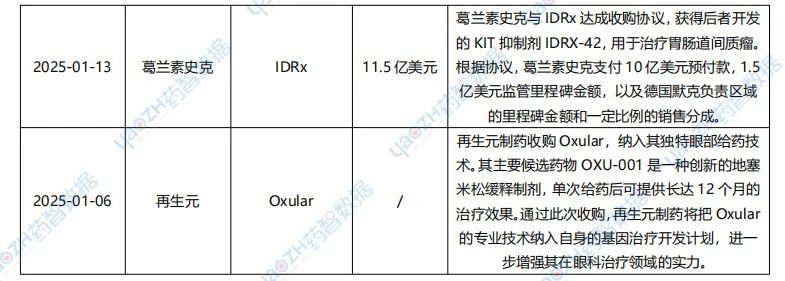
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-投資格局?jǐn)?shù)據(jù)庫
2025年各月全球新藥研發(fā)進(jìn)展完整報(bào)告
