文章來源:藥智新聞
導(dǎo)讀:2025年1月,藥智網(wǎng)收錄整理的國家藥監(jiān)局發(fā)文政策25條
本月國家部委發(fā)文政策情況
2025年1月,藥智網(wǎng)收錄整理的國家藥監(jiān)局發(fā)文政策25條;國家藥審中心發(fā)文政策12條;國家醫(yī)保局發(fā)文政策11條;國家衛(wèi)健委發(fā)文政策16條;醫(yī)療器械技術(shù)審評中心發(fā)文政策5條;國家藥監(jiān)局食品藥品審查核驗(yàn)中心發(fā)文政策3條;國家藥典委員會發(fā)文政策3條;國家市場監(jiān)督管理局發(fā)文政策5條。
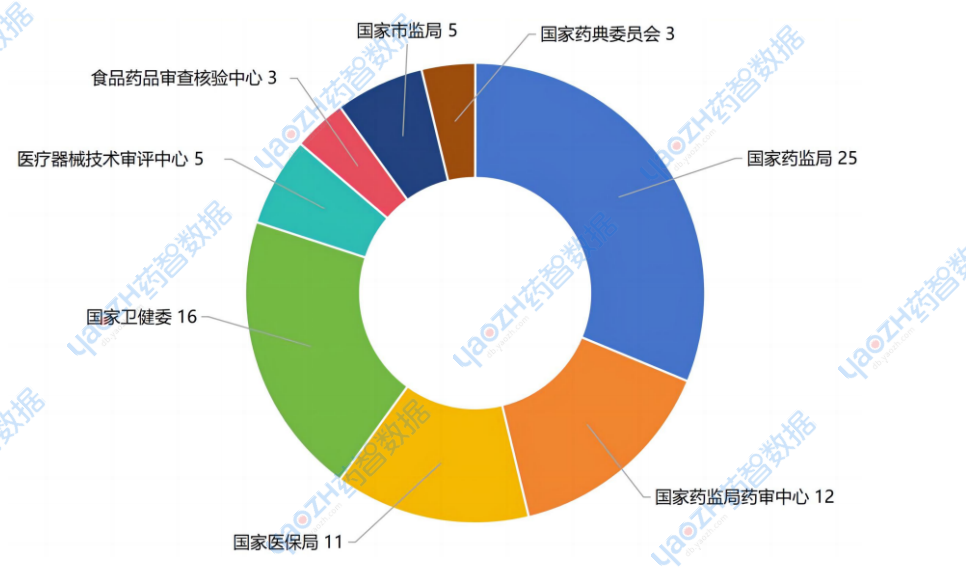
圖1 2025年1月國家部委發(fā)文數(shù)量
數(shù)據(jù)來源:藥智數(shù)據(jù)企業(yè)版-政策法規(guī)數(shù)據(jù)庫
本月醫(yī)藥政策速覽
藥品類
▲1月2日,國家藥監(jiān)局關(guān)于發(fā)布《藥品生產(chǎn)質(zhì)量管理規(guī)范(2010年修訂)》藥用輔料附錄、藥包材附錄的公告(2025年第1號)
該公告制定藥用輔料和藥包材附錄作為配套文件,對藥用輔料、藥包材生產(chǎn)企業(yè)、藥品上市許可持有人提出質(zhì)量管理要求,并規(guī)定藥品監(jiān)管部門的監(jiān)督管理職責(zé),自 2026 年 1 月 1 日起施行。
▲1月2日,國家藥典委員會關(guān)于發(fā)布《國家藥用輔料標(biāo)準(zhǔn)編寫細(xì)則(2025年版)》的通知
在《國家藥用輔料標(biāo)準(zhǔn)編寫細(xì)則(2020年版)》的基礎(chǔ)上修訂形成了《國家藥用輔料標(biāo)準(zhǔn)編寫細(xì)則(2025年版)》。
▲1月3日,國務(wù)院辦公廳關(guān)于全面深化藥品醫(yī)療器械監(jiān)管改革促進(jìn)醫(yī)藥產(chǎn)業(yè)高質(zhì)量發(fā)展的意見
以習(xí)近平新時代中國特色社會主義思想為指導(dǎo),提出到 2027 年和 2035 年的目標(biāo),部署加大研發(fā)創(chuàng)新支持、提高審評審批質(zhì)效、提升產(chǎn)業(yè)合規(guī)水平、擴(kuò)大對外開放合作、構(gòu)建監(jiān)管體系等 5 方面 24 條改革舉措,推動我國從制藥大國向制藥強(qiáng)國跨越,滿足群眾對高質(zhì)量藥品醫(yī)療器械的需求。
▲1月7日,國家衛(wèi)生健康委辦公廳關(guān)于印發(fā)新型抗腫瘤藥物臨床應(yīng)用指導(dǎo)原則(2024年版)的通知
▲1月8日,國家醫(yī)保局發(fā)布關(guān)于對《國家基本醫(yī)療保險、工傷保險和生育保險藥品目錄(2024年)》部分藥品信息進(jìn)行修正的公告
▲1月9日,國家藥監(jiān)局藥審中心關(guān)于發(fā)布《化學(xué)仿制藥口服制劑經(jīng)腸內(nèi)營養(yǎng)管給藥體外對比研究技術(shù)指導(dǎo)原則》的通告(2025年第1號)
▲1月9日,國家藥監(jiān)局藥審中心關(guān)于發(fā)布《治療子宮內(nèi)膜癌新藥臨床研發(fā)技術(shù)指導(dǎo)原則(試行)》的通告(2025年第2號)
▲1月10日,國家藥監(jiān)局藥審中心關(guān)于發(fā)布《抗猴痘病毒藥物臨床試驗(yàn)技術(shù)指導(dǎo)原則(試行)》的通告(2025年第3號)
▲1月14日,國家藥監(jiān)局藥審中心關(guān)于發(fā)布《化藥口服固體制劑中間產(chǎn)品存放時限研究技術(shù)指導(dǎo)原則》的通告(2025年第6號)
▲1月16日,國家藥監(jiān)局藥審中心關(guān)于發(fā)布《放射性治療藥物申報上市臨床風(fēng)險管理計(jì)劃技術(shù)指導(dǎo)原則》的通告(2025年第5號)
▲1月21日,國家藥監(jiān)局關(guān)于簡化港澳已上市傳統(tǒng)口服中成藥內(nèi)地上市注冊審批的公告(2025年第7號)
為貫徹落實(shí)國家建設(shè)粵港澳大灣區(qū)戰(zhàn)略部署,進(jìn)一步支持香港特別行政區(qū)、澳門特別行政區(qū)(以下簡稱香港、澳門特區(qū))中醫(yī)藥事業(yè)發(fā)展,更好融入國家發(fā)展大局,國家藥監(jiān)局對港澳已上市傳統(tǒng)口服中成藥在內(nèi)地上市注冊實(shí)施簡化審批。
▲1月23日,國家藥監(jiān)局藥審中心關(guān)于發(fā)布《預(yù)防用mRNA疫苗非臨床研究技術(shù)指導(dǎo)原則》的通告(2025年第7號)
醫(yī)療器械類
▲1月6日,國家藥監(jiān)局關(guān)于廢止YY/T 0771.1-2020 《動物源醫(yī)療器械 第1部分:風(fēng)險管理應(yīng)用》和YY/T 0771.2-2020 《動物源醫(yī)療器械 第2部分:來源、收集與處置的控制》醫(yī)療器械行業(yè)標(biāo)準(zhǔn)的公告(2024年第157號)
為進(jìn)一步優(yōu)化醫(yī)療器械標(biāo)準(zhǔn)體系,國家藥品監(jiān)督管理局決定廢止YY/T 0771.1-2020 《動物源醫(yī)療器械 第1部分:風(fēng)險管理應(yīng)用》和YY/T 0771.2-2020 《動物源醫(yī)療器械 第2部分:來源、收集與處置的控制》2項(xiàng)醫(yī)療器械行業(yè)標(biāo)準(zhǔn)。
▲1月7日,國家藥監(jiān)局發(fā)布《醫(yī)療器械監(jiān)督管理?xiàng)l例(國務(wù)院令第276號)》
條例內(nèi)容根據(jù)2024年12月6日《國務(wù)院關(guān)于修改和廢止部分行政法規(guī)的決定》第二次修訂。
▲1月15日,國家藥監(jiān)局綜合司公開征求《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范(修訂草案征求意見稿)》意見,1月16日,國家藥監(jiān)局食品藥品審核查驗(yàn)中心發(fā)布《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》修改前后對照表
國家藥監(jiān)局于2025年1月15日在官網(wǎng)發(fā)布文件,向社會公開征求《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范(修訂草案征求意見稿)》意見建議。為便于監(jiān)管部門和企業(yè)理解修訂草案征求意見稿和2014年版《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》的主要變化,核查中心組織對新舊版本《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》進(jìn)行了對比,現(xiàn)全文刊登如下,供廣大監(jiān)管人員和業(yè)界從業(yè)人員研究參考。
其他
▲1月10日,國家衛(wèi)生健康委辦公廳關(guān)于印發(fā)《國家衛(wèi)生健康委主責(zé)國家重點(diǎn)研發(fā)計(jì)劃重點(diǎn)專項(xiàng)管理實(shí)施細(xì)則》的通知
為規(guī)范國家衛(wèi)生健康委主責(zé)的國家重點(diǎn)研發(fā)計(jì)劃重點(diǎn)專項(xiàng)管理,保障專項(xiàng)組織實(shí)施,根據(jù)黨中央、國務(wù)院關(guān)于國家科技計(jì)劃管理改革的有關(guān)要求,以及科技部、財(cái)政部的相關(guān)暫行辦法,制定并實(shí)施該細(xì)則,以實(shí)現(xiàn)高效、科學(xué)、規(guī)范和公正的管理,確保重點(diǎn)專項(xiàng)順利實(shí)施并取得成效。
▲1月11日,國家醫(yī)療保障局關(guān)于開展2025年定點(diǎn)醫(yī)藥機(jī)構(gòu)違法違規(guī)使用醫(yī)保基金自查自糾工作的通知
為持續(xù)推進(jìn)醫(yī)保基金安全規(guī)范使用,國家醫(yī)保局決定在全國范圍內(nèi)開展定點(diǎn)醫(yī)藥機(jī)構(gòu)自查自糾工作。此次自查自糾工作涵蓋了定點(diǎn)醫(yī)療機(jī)構(gòu)和定點(diǎn)零售藥店,重點(diǎn)檢查腫瘤、麻醉、重癥醫(yī)學(xué)等9個領(lǐng)域,要求各級醫(yī)保部門制定并細(xì)化問題清單,組織轄區(qū)內(nèi)所有定點(diǎn)醫(yī)藥機(jī)構(gòu)進(jìn)行自查自糾,確保醫(yī)保基金的合理規(guī)范使用。
▲1月13日,國家藥監(jiān)局食品藥品審核查驗(yàn)中心關(guān)于發(fā)布《細(xì)胞治療產(chǎn)品生產(chǎn)檢查指南》的通告
▲1月14日,市場監(jiān)管總局關(guān)于發(fā)布《特殊醫(yī)學(xué)用途全營養(yǎng)配方食品注冊指南》的公告
▲1月17日,國家藥監(jiān)局食品藥品審核查驗(yàn)中心關(guān)于發(fā)布《清潔驗(yàn)證技術(shù)指南》的通告
▲1月22日,國家衛(wèi)健委《關(guān)于印發(fā)流行性感冒診療方案(2025年版)的通知》
▲1月23日,國家藥監(jiān)局藥審中心關(guān)于發(fā)布《疫苗說明書臨床相關(guān)信息撰寫指導(dǎo)原則(試行)》的通告(2025年第9號)
▲1月23日,國家醫(yī)療保障局發(fā)布《關(guān)于建立醫(yī)保數(shù)據(jù)工作組更好賦能醫(yī)療機(jī)構(gòu)發(fā)展的通知》
國家醫(yī)保局決定建立醫(yī)保數(shù)據(jù)工作組,旨在通過數(shù)據(jù)賦能提升醫(yī)療、醫(yī)保、醫(yī)藥的協(xié)同發(fā)展和治理能力,加強(qiáng)醫(yī)保部門與定點(diǎn)醫(yī)療機(jī)構(gòu)的 信息互通和改革協(xié)同,優(yōu)化醫(yī)保基金管理,提高基金使用效率,促進(jìn)醫(yī)療機(jī)構(gòu)內(nèi)部管理和服務(wù)行為的規(guī)范化,從而推動醫(yī)保醫(yī)療改革的深入發(fā)展。
▲1月24日,國家藥監(jiān)局醫(yī)療器械技術(shù)審評中心發(fā)布關(guān)于第二次公開征求《體外診斷試劑變更注冊審查指導(dǎo)原則(征求意見稿)》意見的通知
▲1月27日,國家醫(yī)療保障局辦公室關(guān)于印發(fā)《按病種付費(fèi)醫(yī)療保障經(jīng)辦管理規(guī)程(2025版)》的通知
為貫徹落實(shí)《中共中央國務(wù)院關(guān)于深化醫(yī)療保障制度改革的意見》,根據(jù)《國家醫(yī)療保障局辦公室關(guān)于印發(fā)按病組和病種分值付費(fèi)2.0版分組方案并深入推進(jìn)相關(guān)工作的通知》要求,深化醫(yī)保支付方式改革,提高醫(yī)療保障基金使用效率,保障參保人員權(quán)益,做好按病種付費(fèi)經(jīng)辦管理工作,現(xiàn)制定本規(guī)程。
▲1月27日,國家醫(yī)療保障局發(fā)布《關(guān)于有序推進(jìn)省內(nèi)異地就醫(yī)住院費(fèi)用納入按病種付費(fèi)管理的通知》
為貫徹落實(shí)黨的二十大和二十屆二中、三中全會精神,深化醫(yī)保支付方式改革,規(guī)范異地就醫(yī)醫(yī)療服務(wù)行為,促進(jìn)合理診療、因病施治,推動建立統(tǒng)一規(guī)范、內(nèi)外協(xié)同、統(tǒng)籌平衡、安全高效的異地就醫(yī)醫(yī)保支付機(jī)制,決定在全國范圍內(nèi)有序推進(jìn)省內(nèi)異地就醫(yī)住院費(fèi)用納入按病種付費(fèi)管理。
